随着工业的发展,汞污染越来越严重。由于汞的污染特性,不易分解及转移。造成了食品中富集了各种含汞化合物,从而导致各种慢性、急性汞中毒事件频出。目前,食品中汞的主要存在形式可分为无机汞和有机汞两大类,其中有机汞的毒性远大于无机汞,无机汞主要是对肾脏有毒性作用,而有机汞主要对脑组织伤害比较大。因此对汞形态的监测显得尤为重要。
本文参考国家卫生和计划生育委员会发布的《GB 5009.17-2014 食品中甲基汞的测定》,通过HPLC-ICPMS联用,������采用C18柱,利用等度洗脱的方式对稀酸浸提后的大�����米进行了分析,同时对样品采取了加标处理,且加标回收率良好。测试结果表明,该方法能够快速准确地进行大米样品中汞形态的分析。
1.仪器简介
本方法采用Skyray Instrument LC-310E与ICP-MS 2000E联用,采用一键式数据采集、精准式谱图定位及强大的软件谱图处理功能,可满�����足不同的形态测试需求(如图1)。

图1.HPLC-ICPMS联用测汞形态的分析仪
2.测试原理
样品溶液经过前处理,由HPLC进样口进样,经色谱柱分离,通过雾化器雾化后送入高温等离子体中,干燥、原子化、电离,元素离子经接口室进入质谱仪,通过离子透镜系统、质量分析器及检测器,检测器对相应元素离子做出响应(每秒离子计数cps(counts
per second),经软件处理,响应强度和时间组成的峰面积与相应组分离子浓度成正比������关系进行定性定量分析。
3.实验部分
3.1实验设备及试剂
液相色谱-电感耦合等离子体质谱联用仪(和记官网·[app]官方网站
�������
);
电子天平(BSA224S,赛多利斯);
色谱柱(Ultimate XB-C18,4.6×150mm,5μm);
超纯水系统(Millipore,电阻率为18.25MΩ·cm);
盐酸(优级纯,Scharlau);
氨水(优级纯,上海晶纯试剂有限公司);
乙酸铵(优级纯,阿拉丁化学试剂);
L-半胱氨酸(生物纯,阿拉丁化学试剂);
甲醇(色谱纯,Oceanpak 色谱纯试剂);
汞形态标准溶液(水中汞GBW(E)083186、甲基汞GBW(E)083364、乙基汞GBW(E)081524,中国计量科学院);
超声波(KH-500E,昆山禾创);
双功能水浴恒温振荡器(SHA-B,江苏国华);
高速离心机(TG16G,凯特)。
3.2样品前处理
称取大米样品1.0g(精确至0.001g),置于15mL的离心管中,加入10mL的盐酸溶液(5mol/L)静置过夜。后经常温水浴振荡60min,于4℃下以8000r/min的转速进行离心15min。取上层清液2mL至5mL的容量瓶中,用�������稀氨水调节PH到7.0,再加入0.1mL的L-半胱氨酸(10g/L),最后用超纯水定容至刻度并摇匀。用0.45μm的有机系滤膜过滤后,待测。
3.3流动相及汞形态标准溶液配制
3.3.1流动相的配制
60mmol/L乙酸铵+0.1%L-半胱氨酸+5%甲醇:称取4.627g乙酸铵,1.21gL-����半胱氨酸于100mL容量瓶中,加入少量的超纯水并于电热板上加热使其完全溶解,冷却后定容至100mL。将定容好的溶液移入1000mL的淋洗液瓶中,同时加入50mL的甲醇,定容至1L。经0.45μ����m的有机系滤膜过滤后,于超声波超声脱气30min,现用现配。
3.3.2汞形态标准溶液:
三种汞标准溶液采用淋洗液按照梯度浓度的方式依次被稀释为1.0µg/L、2.0.µg/L、4.0µg/L、8.0µg/L、10.0µg/L 混合��������标准溶液,同时配������制5µg/L三种汞形态的单标溶液,用来判别每种汞形态的出峰时间。
3.4实验条件
3.4.1色谱条件
色谱条件详见表1。
表1. HPLC分析条件
|
参数
|
参数设定
|
|
色谱柱
|
Ultimate XB-C18,5μm,150×4.6mm。
|
|
流动相
|
60mmol/L乙酸铵+0.1%L-半胱氨酸+5%甲醇(pH=7.0)。
|
|
流 速
|
1.0mL/min
|
|
柱 温
|
25℃
|
|
进样量
|
100μL
|
|
洗脱程序
|
等度洗脱
|
3.4.2质谱条件
ICP-MS分析条件见表2。
表2.ICP-MS分析条件
|
参数
|
参数设定
|
参数
|
参数设定
|
|
功 率
|
1300W
|
等离子气
|
13L/min
|
|
辅助气
|
1.06L/min
|
载 气
|
1.2L/min
|
|
采样深度
|
16
|
分析模式
|
标准模式
|
|
待测质量数
|
202
|
驻留时间
|
10ms
|
3.5实验结果
3.5.1标准曲线
按照混合标准溶液浓度1.0µg/L、2.0.µg/L、4.0µg/L、8.0µg/L、10.0µg/L 进样得到色谱图,计算其峰面积,以浓度和峰面积绘制标准曲线,线性相关系数均大于0.999,结果详见图2-1~2-3。

图2-1.Hg2+标准曲线
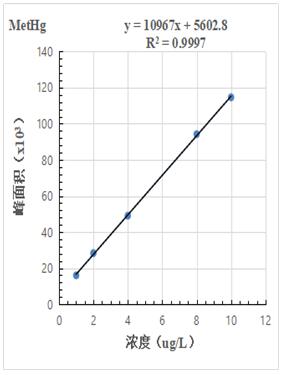
图2-2.MetHg标准
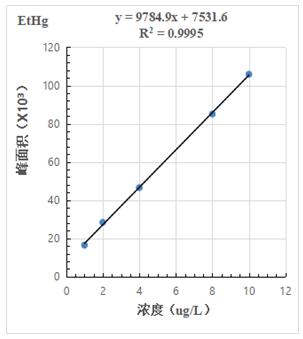
图2-3.EtHg标准曲线
3.5.2色谱分离图
1.0µg/L、2.0.µg/L、4.0µg/L、8.0µg/L、10.0µg/L 汞形态混合标准溶液分离色图谱如图3所示,其中无机汞(Hg2+)、甲基汞(MetHg)、乙基汞(EtHg)相对保留时间分别为118s、185s、379s,从谱图叠加图上可以看出,三种汞形态出峰时间稳定,且分离度较好。
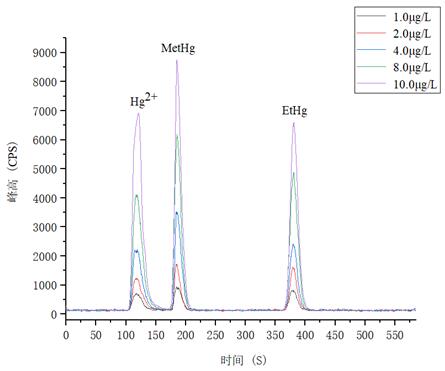
图3. 汞形态混合标准溶液分离图谱
3.5.3 检出限
&nb�������sp; 如图4所示为1.0µg/L汞形态混和标准溶液分离图谱,以各形态峰附近基线处的3倍信噪比(S/N)峰高对应的浓度作为检出限,溶液中Hg2+、MetHg、EtHg分别为0.112µg/L、0.0718µg/L、0.0698µg/L。
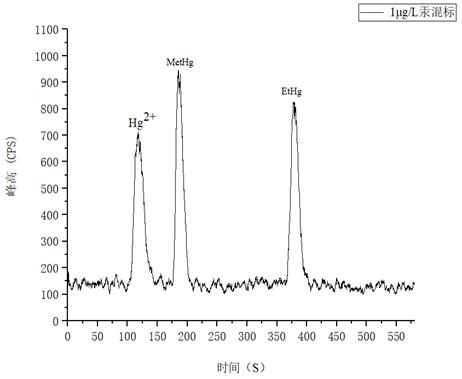
图4. 1.0µg/L汞形态混合标准溶液图谱
3.5.4 测试结果
以大米样品为试样,进行稀酸浸提,同时为了考察方法的准确性,并对大米试样采取了加标的方式,测试���������结果详�������见表3。
表3 大米样品及样品加标结果
|
组分名称
|
稀释后浓度
|
原液浓度
|
加标后浓度
|
加标回收率
|
|
(µg/L)
|
(µg/kg)
|
(µg/L)
|
(%)
|
|
无机汞
|
0.227
|
5.68
|
5.84
|
112
|
|
甲基汞
|
未检出
|
ND
|
4.50
|
90
|
|
乙基汞
|
未检出
|
ND
|
4.67
|
93
|

图5. 大米样品及样品加标5.0µg/L图谱
4. 结论
本�������文建立了LC-ICPMS测试大米中汞形态的分析方法,结果表明该方法检出限低、测试结果准确,其加标回收率在90%~112%之间,线性相关系数均在0.999以上;同时汞的三种形态能够在8min左右完成,且分离度较好,该方法可满足食品中大米样品汞形态分析的要求。
5.参考文献
[1] 国家卫生和计划生育委员会发布 GB 5009.17-2014食品安全国家标准 食品中甲基汞的测定 液相色谱-原子荧光光������谱联用方法,2015。